Размерность скорости химической. Константа скорости реакции

Методические указания к лабораторной работе
По дисциплине ""Химия"" для студентов
Составитель В.С. Аксенов
Рецензент
Доктор химических наук, профессор Ф.Ф. Ниязи
Скорость химических реакций : Методические указания к лабораторной работе по дисциплине ""Химия"" / Курск. гос. техн. ун-т; Сост. В.С.Аксенов. Курск, 2003. 20 с.
Излагаются методические материалы по изучению темы ""Скорость химических реакций"", расчету скоростей в химических реакциях и выполнению лабораторной работы.
Предназначены для студентов всех специальностей, изучающих общую химию
Табл. 2. Ил. 2.
ИД № 06430 от 10.12.01.
Подписано в печать. Формат 60х84 1/16. Печать офсетная. Усл.печ.л. 1,16. Уч.-изд.л. 1,05. Тираж 50 экз. Заказ
Курский государственный технический университет.
Издательско-полиграфический центр Курского государственного технического университета. 305040 Курск, ул. 50 лет Октября, 94.
Контрольные вопросы по теме
1. Что такое скорость химической реакции? В каких единицах она измеряется?
2. Что такое истинная и средняя скорость реакции?
3. Что такое кинетическое уравнение реакции (закон действующих масс)?
4. Как записывается кинетическое уравнение для гомогенной реакции?
5. Каковы особенности гетерогенные реакций?
6. Что такое кинетический, диффузионный и смешанный контроль в гетерогенных реакциях?
7. Какие существуют формы записи для кинетических уравнений гетерогенных реакций?
8. Что такое константа скорости реакции? Какие условия проведения реакции влияют, а какие не влияют на величину константы скорости?
10 . Когда влияет давление на скорость химической реакции?
12 . Как влияет температура на скорость химической реакции? Приведите уравнение Вант-Гоффа.
13 . Что такое температурный коэффициент реакции?
14 . Что такое катализ? На какие параметры процесса действует катализатор?
Скорость химических реакций.
Кинетика ― учение о скорости различных процессов, в том числе химических реакций. Одним из основных понятий в химической кинетике является скорость реакции.
Скоростью химической реакции V называют изменение количества реагирующего вещества за единицу времени в единице реакционного пространства .
В гомогенной системе реакционным пространством служит объем сосуда, в котором протекает взаимодействие, а количество вещества в единице объёма называется концентрация С и выражается в моль/л .
Поэтому с случае гомогенного процесса, протекающего при постоянном объёме, скорость гомогенной химической реакции измеряется изменением концентрации какого-либо из реагирующих веществ за единицу времени .
Обычно время τ выражается в сек, поэтому размерность скорости реакции как правило,моль/л·сек . При химическом взаимодействии концентрация каждого из исходных веществ уменьшается во времени (С 2 <С 1 , ΔС<0) , а концентрация каждого из продуктов реакции возрастает (С 2 >С 1 , ΔС>0) . Изменение концентраций исходных веществ и продуктов реакции во времени приведено на рис.1. В химической кинетике различают среднюю и истинную (или мгновенную) скорость реакции. Средняя скорость v равна отношению ΔС/Δτ (ΔС = С 2 -С 1 , Δτ = τ 2 -τ 1 ) . Чтобы величина скорости была всегда положительной, перед дробью ставят знаки ""±"".
V = ± -–-
Δτ
Истинная скорость химической реакции V ист определяется пределом, к которому стремится отношение ΔС/Δτ при τ → 0, т.е. производной концентрации по времени:
V ист = ± -–-
dτ
Зависимость скорости реакции от концентрации реагентов. Необходимым условием для осуществления акта химического взаимодействия между молекулами должно быть их столкновение. Столкновение молекул в некотором реакционном пространстве при заданной температуре происходят тем чаще, чем больше этих молекул. Поэтому скорость химической реакции зависит от концентрации реагирующих веществ. По мере уменьшения концентрации исходных веществ во времени (рис.1, кривая 1) скорость реакции падает.
Количественно зависимость скорости реакции от концентрации реагирующих веществ выражается законом действующих масс , который в современной формулировке выглядит так:
при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции .
Для реакции а А + b В → m М + n N
математическое выражение закона действующих масс имеет вид:
V = k С А а ·С В b (1)
где V ― скорость реакции; С А и С В ― концентрации реагентов А и В; а , b ― стехиометрические коэффициенты в уравнении реакции; k ― коэффициент пропорциональности, называемый константой скорости химической реакции. Размерность константы скорости определяется величинами стехиометрических коэффициентов а и b и остается такой, чтобы скорость V имела размерность моль/л∙сек . Если нет точных данных, размерность k принимают сек ―1 . При С А = С В = 1 моль/л k численно равнаV . Выражение (1) называют также кинетическим уравнением реакции .
Константа скорости химической реакции k определяется природой реагирующих веществ и зависит от температуры, от присутствия катализатора, но не зависит от концентрации веществ, участвующих в реакции.
Пример 1 . В реакционный сосуд объемом 2 л помещены 0,06 моль вещества А и 0,02 моль вещества В. При определенной температуре протекает реакция А + 2В = АВ 2 Найти значение константы скорости реакции при этой температуре, если при заданных концентрациях веществ А и В скорость реакции равна 6·10 ―7 моль/(л·сек) .
Решение: Зная количества реагирующих веществ и объем системы, найдем молярные концентрации реагентов:
С А = 0,06/2 = 0.03 = 3·10 ―2 моль/л ; С В = 0,02/2 = 0.01 = 10 ―2 моль/л
Запишем выражение кинетического уравнения, связывающего скорость реакции с концентрациями реагирующих веществ:
V = k С А ·С В 2
V 6.10 ―7
Отсюда: k = ----- = ------- = 0,2 л 2 /(моль) 2 ∙сек
С А ·С В 2 · 3·10 ―2 (10 ―2) 2
Закон действующих масс справедлив только для наиболее простых по своему механизму взаимодействий, протекающих в газах или в разбавленных растворах. Сложные реакции могут быть совокупностью параллельно или последовательно протекающих процессов. Закон действующих масс справедлив для каждой отдельной стадии реакции, но не для всего взаимодействия в целом. Та стадия процесса, скорость которой минимальна, лимитирует скорость реакции в общем. Поэтому математическое выражение закона действующих масс, записанное для самой медленной (лимитирующей) стадии процесса, приложимо одновременно и ко всей реакции в целом.
Если в реакции участвуют два или более веществ, то скорость реакции может зависеть от концентрации только одного из них, участвующего в самой медленной стадии процесса и не зависеть от концентрации других.
Скорость гетерогенных химических реакций. Многие химические процессы, имеющие большое значение в технике, относятся к числу гетерогенных реакций. Один или несколько компонентов процесса находятся в конденсированной, обычно твердой фазе. Концентрации твердых веществ не записываются в кинетическое уравнение (закон действующих масс) . Условно эти концентрации принимают постоянными и равными 1. Это первая особенность гетерогенных реакций. Они идут на поверхности раздела фаз, которая и является их реакционным пространством. Поэтому второй особенностью кинетики этих реакций является влияние площади реакционной поверхности на скорость реакции. Так для реакции:
Fе 2 О 3(К) + 3СО (Г) → 2Fе + 3СО 2(Г)
кинетическое уравнение может быть записано в виде: V = k∙С 3 СО ∙S , где С СО ― молярная концентрация монооксида углерода СО (Г) , единственного газообразного компонента в реагирующих исходных веществах, S ― площадь поверхности, на которой идет реакция. Твердое вещество Fе 2 О 3(К) в кинетическое уравнение не записывается. Скорости гетерогенных химических реакций имеют размерность моль/л∙сек∙м 2
Однако в большинстве случаев площадь реакционной поверхности практически невозможно измерить и она непосредственно не фигурирует в кинетическом уравнении (законе действующих масс). Она
""запрятывается"" в константу скорости k и это учитывается в размерности константы скорости.
Пример 2 . Для реакции: Si (ТВ) + 2Н 2 О (Г) SiО 2(ТВ) + 2Н 2(Г) напишите выражение для кинетического уравнения.
Решение: Данная реакция гетерогенная, протекает на границе раздела фаз. Из реагирующих веществ вода участвует в реакции в газообразной форме, перед ней коэффициент в уравнении равен 2 (…+ 2Н 2 О (Г) ). Кремний (Si (ТВ) ) ― твердое вещество, поэтому его концентрацию не учитываем в кинетическом уравнении. Следовательно, кинетическое уравнение (закон действующих масс) для данной реакции может иметь вид: V = k·С 2 Н 2 О . Размерность константы скорости в этом случае л/моль∙сек∙м 2 .
В процессе реакции уменьшается концентрация реагента в зоне реакции C S по сравнению с его концентрацией в в объеме C V из-за расхода реагента. Поэтому скорость гетерогенной химической реакции зависит от скорости подвода реагентов в зону химической реакции ,
что является третьей особенностью этих реакций.
Наибольшее изменение концентрации реагента происходит в тонком слое около реакционной поверхности, называемом диффузионны ом слоем. Перенос вещества здесь происходит в основном за счет диффузии.
Если скорость диффузии много больше скорости реакции (V Д >> V ), то реагенты без проблем подаются в реакционное пространство, к поверхности, все законы влияния концентрации на скорость, описанные выше, соблюдаются. Для таких случаев есть выражение «кинетический контроль реакции ». Если скорости химической реакции и диффузии сопоставимы, имеет место смешанный контроль . И, наконец, когда скорость диффузии много меньше скорости реакции (V Д << V ) то говорят о диффузионном контроле реакции.
В этом случае может наблюдаться нулевой
порядок реакции по всем реагентам. Это
значит, что в координатахV
―
C
скорость
не зависит от концентраций реагентов,
а зависит от скорости диффузии, величины
поверхности и температуры, которые не
входят в кинетическое уравнение. Такое
явление может иметь место при реакции
на твердой поверхности в жидких средах
с высокой вязкостью. Однако большинство
гетерогенных реакций имеет порядок,
отличающийся от нулевого, нередко
дробный. На рис. 2 приведены графические
формы возможных зависимостей скорости
реакции от концентраций реагентов.
этом случае может наблюдаться нулевой
порядок реакции по всем реагентам. Это
значит, что в координатахV
―
C
скорость
не зависит от концентраций реагентов,
а зависит от скорости диффузии, величины
поверхности и температуры, которые не
входят в кинетическое уравнение. Такое
явление может иметь место при реакции
на твердой поверхности в жидких средах
с высокой вязкостью. Однако большинство
гетерогенных реакций имеет порядок,
отличающийся от нулевого, нередко
дробный. На рис. 2 приведены графические
формы возможных зависимостей скорости
реакции от концентраций реагентов.
Зависимость скорости реакций от давления в системе. В тех случаях, когда среди реагирующих веществ имеются газы, скорость реакций зависит от давления в системе. При повышении давления пропорционально возрастает число молекул газа в единице объема, что эквивалентно повышению концентрации данного газа.
Пример 3. Как изменится скорость реакции 2NО + О 2 → 2NО 2 при уменьшении объема замкнутой системы в два раза при постоянной температуре?
Решение. Уменьшение объема в замкнутой системе эквивалентно пропорциональному увеличению давления, так как, согласно закону Менделеева-Клайперона РW = νRТ. (Здесь W ― объем системы.)
Кинетическое уравнение данной реакции имеет вид: V = k С 2 NО ·С О 2
При уменьшении объема системы в два раза и связанным с этим повышении давления в два раза концентрации реагирующих веществ тоже повышаются в два раза: С" NО = 2С NО С" О 2 = 2С О 2
Новая скорость реакции:
V" = k С" NО 2 ·С" О 2 = k (2 С NО ) 2 ·(2С О 2 ) = 8 k С NО 2 ·С О 2 = 8V
Вывод. При уменьшении объема замкнутой системы в два раза при постоянной температуре скорость данной реакции повышается в 8 раз.
Зависимость константы скорости реакции от температуры . Большинство реакций ускоряется при нагревании. Температура действует непосредственно на константу скорости k . Пусть V 1 ― скорость реакции при температуре Т 1 , а V 2 ― скорость этой же реакции при температуре Т 2 (Т 1 <Т 2 ) . В таком случае имеет место эмпирическое правило Вант-Гоффа.

где γ – температурный коэффициент, показывающий во сколько раз повысится скорость реакции при повышении температуры на 10 0 С. Для большинства реакций при температурах, близких к комнатной, γ составляет величину 2-4.
Уравнение Вант-Гоффа широко используется, однако следует помнить, что оно эмпирическое приблизительное, его можно применять только для ориентировочных расчетов.
Пример 4. При 100 0 С некоторая реакция заканчивается за 20 мин. Принимая температурный коэффициент скорости реакции γ = 3,5, рассчитайте, через какое время закончится реакция при 60 0 С
Решение . Скорость реакции, как и скорость всякого процесса, обратно пропорциональна времени проведения процесса. Следовательно, V 2 /V 1 = τ 1 /τ 2 . Пусть Т 1 , V 1 и τ 1 ― параметры медленного (низкотемпературного) процесса, а Т 2 , V 2 и τ 2 ― параметры высокотемпературного процесса. Подставляем имеющиеся данные в уравнение Вант-Гоффа:
V 2 /V 1 = 3,5 (100 ― 60)/10 = (3,5) 4 = 150. Так как V 2 /V 1 = τ 1 /τ 2 = 150,
τ 1 /τ 2 = τ 1 /20 τ 1 = 150·20 = 3000 мин = 50 часов.
Одним из методов ускорения химической реакции является катализ , который осуществляется при помощи веществ (катализаторов), увеличивающих скорость реакции, но не расходующихся в результате ее протекания. Как и при повышении температуры, при введении катализатора повышается константа скорости реакции . Механизм действия катализатора сводится к уменьшению величины энергии активации реакции, т.е. к уменьшению разности между средней энергией активных молекул (активного комплекса) и средней энергией молекул исходных веществ. Скорость химической реакции при этом резко повышается
Вопрос№3
От каких факторов зависит константа скорости химической реакции?
Константа скорости реакции (удельная скорость реакции ) - коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль /л.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, от присутствия в системе катализатора, но не зависит от их концентрации.
1. Температура. При повышении температуры на каждые 10°C скорость реакции возрастает в 2-4 раза (Правило Вант-Гоффа) . При увеличении температуры от t1 до t2 изменение скорости реакции можно рассчитать по формуле: (t2 - t1) / 10 Vt2 / Vt1 = g (где Vt2 и Vt1 - скорости реакции при температурах t2 и t1 соответственно; g- температурный коэффициент данной реакции) . Правило Вант-Гоффа применимо только в узком интервале температур. Более точным является уравнение Аррениуса: k = A e –Ea/RT где A - постоянная, зависящая от природы реагирующих веществ; R - универсальная газовая постоянная ; Ea - энергия активации, т. е. энергия, которой должны обладать сталкивающиеся молекулы, чтобы столкновение привело к химическому превращению. Энергетическая диаграмма химической реакции. Экзотермическая реакция Эндотермическая реакция А - реагенты, В - активированный комплекс (переходное состояние) , С - продукты. Чем больше энергия активации Ea, тем сильнее возрастает скорость реакции при увеличении температуры. 2. Поверхность соприкосновения реагирующих веществ. Для гетерогенных систем (когда вещества находятся в разных агрегатных состояниях) , чем больше поверхность соприкосновения, тем быстрее протекает реакция. Поверхность твердых веществ может быть увеличена путем их измельчения, а для растворимых веществ - путем их растворения. 3. Катализ. Вещества, которые участвуют в реакциях и увеличивают ее скорость, оставаясь к концу реакции неизменными, называются катализаторами. Механизм действия катализаторов связан с уменьшением энергии активации реакции за счет образования промежуточных соединений. При гомогенном катализе реагенты и катализатор составляют одну фазу (находятся в одном агрегатном состоянии) , при гетерогенном катализе - разные фазы (находятся в различных агрегатных состояниях) . Резко замедлить протекание нежелательных химических процессов в ряде случаев можно добавляя в реакционную среду ингибиторы (явление "отрицательного катализа").
Вопрос№4
Сформулируйте и запишите закон действующих масс для реакции:
2 NO+O2=2NO2
ЗАКОН ДЕЙСТВУЮЩИХ МАСС: скорость химической реакции пропорциональна произведению концентраций реагирующих веществ. для реакции 2NO + O2 2NO2, закон действующих масс запишется так: v=kС2(NO)·С (O2), где k – константа скорости, зависящая от природы реагирующих веществ и температуры. Скорость в реакциях с участием твердых веществ определяется только концентрацией газов или растворенных веществ: С+О2=СО2, v =kCO2
Общая химия: учебник / А. В. Жолнин; под ред. В. А. Попкова, А. В. Жолнина. - 2012. - 400 с.: ил.
Глава 2. ОСНОВЫ КИНЕТИКИ ХИМИЧЕСКИХ РЕАКЦИЙ
Глава 2. ОСНОВЫ КИНЕТИКИ ХИМИЧЕСКИХ РЕАКЦИЙ
Разница между дыханием и горением только в скорости процесса.
А.-Л. Лавуазье
2.1. ХИМИЧЕСКАЯ КИНЕТИКА. ПРЕДМЕТ И ОСНОВНЫЕ ПОНЯТИЯ ХИМИЧЕСКОЙ КИНЕТИКИ. СКОРОСТЬ РЕАКЦИИ
О направлении, глубине и принципиальной возможности протекания процесса судят по величине изменения свободной энергии (ΔG ≤0). Однако эта величина не говорит о реальной возможности протекания реакции в данных условиях.
Например, реакция взаимодействия закиси азота с кислородом протекает мгновенно при комнатной температуре:
В то же время 2Н 2 (г) + О 2 (г) = 2Н 2 О(ж), Δ°G = -286,8 кДж/моль - реакция, характеризующаяся значительно большим уменьшением свободной энергии, в обычных условиях взаимодействие не протекает, но при 700 °С или в присутствии катализатора процесс протекает мгновенно. Следовательно, термодинамика не отвечает на вопрос условий и скорости протекания процесса. В этом проявляется ограниченность термодинамического подхода. Для описания химической реакции необходимо знать также закономерности ее протекания во времени, которые изучает кинетика.
Кинетика - это раздел химии, изучающий скорость, механизм химических реакций и влияние на них различных факторов.
В зависимости от того, в одной или нескольких фазах находятся компоненты реакции, различают кинетику гомогенных и гетерогенных реакций. По механизму реакции делятся на простые и сложные, поэтому выделяют кинетику простых и сложных реакций.
Основным понятием кинетики реакции является скорость химической реакции. Определение скорости химических реакций имеет биологическое и народно-хозяйственное значение.
Скорость химической реакции определяется количеством вещества, прореагировавшего за единицу времени в единице объема (в случае гомогенных реакций, когда реагирующие вещества находятся в одной фазе) или на единице поверхности раздела фаз (в случае гетерогенных реакций, когда реагирующие вещества находятся в различных фазах).
Скорость реакции характеризуют изменением концентрации какого-либо из исходных или конечных продуктов реакции в функции времени. Уравнение, описывающее зависимость скорости реакции (v) от концентрации (с) реагирующих веществ, называется кинетическим. Скорость реакции чаще выражают в моль/л-с, в биохимии в мг/100мл-с, или в массовой доле, в %/100 мл-с. Различают среднюю скорость реакции в интервале времени и истинную скорость реакции в определенный момент времени. Если в интервале времени t 1 и t 2 концентрация одного из исходных веществ или продуктов реакции равна соответственно с 1 и с 2 , то среднюю скорость реакции (v) в интервале времени t 1 и t 2 можно выразить:
Поскольку речь идет в данном случае об убыли концентрации исходного вещества, т.е. изменение концентрации вещества берется в этом случае со знаком «минус» (-). Если скорость реакции оценивается изменением (увеличением) концентрации одного из продуктов реакции, то со знаком «плюс» (+):
По уравнению (2.2) определяют среднюю скорость химической реакции. Истинную (мгновенную) скорость реакции определяют графически. Строят график зависимости концентрации исходного вещества или продукта реакции (Са) от времени (t) - кинетическую кривую реакции Са - f(t) для нелинейного процесса (рис. 2.1).
В каждый момент времени (например, t 1) истинная скорость реакции равна тангенсу угла наклона касательной к кинетической кривой в точке, соответствующей данному моменту времени. Согласно графику мгновенная скорость реакции будет рассчитываться по формуле:
В биохимии для описания кинетики ферментативных реакций используется уравнение Михаэлиса- Ментен, которое показывает зависимость скорости реакции, катализируемой ферментом, от концентрации субстрата и фермента. Простейшая кинетическая схема, для которой справедливо уравнение Михаэлиса: E + S ↔ ES → E + P:

Рис. 2.1. Кинетическая кривая
где V m - максимальная скорость реакции; К м - константа Михаэлиса, равная концентрации субстрата, при которой скорость реакции составляет половину от максимальной; S - концентрация субстрата.
Исследование скорости химической реакции позволяют получить информацию о ее механизме. Помимо концентрации скорость реакции зависит от природы реагентов, внешних условий и наличия катализатора.
2.2. МОЛЕКУЛЯРНОСТЬ И ПОРЯДОК РЕАКЦИИ. ПЕРИОД ПОЛУПРЕВРАЩЕНИЯ
В кинетике химические реакции различаются по признаку моле-кулярности и порядка реакции. Молекулярность реакции определяется числом частиц (атомов, молекул или ионов), одновременно участвующих в элементарном акте химического превращения. В элементарном акте реакции могут принимать участие одна, две или три молекулы. Вероятность соударения большего числа частиц очень мала. По этому признаку различают мономолекулярные, бимолекулярные и тримоле-кулярные реакции. Экспериментально молекулярность реакции можно определить только для элементарных (простых) реакций, протекающих в одну стадию в соответствии со стехиометрическим уравнением. Для протекания большинства подобных реакций требуется большая энергия активации (150-450 кДж/моль).
Большая часть реакций - сложные. Совокупность элементарных стадий, составляющих сложную реакцию, называется механизмом реак-
ции. Поэтому для характеристики кинетики реакции вводится понятие порядка реакции, который определяется по стехиометрическому уравнению.
Сумма стехиометрических показателей всех исходных веществ, входящих в уравнение реакции (2.5) (a + b), определяет общий порядок реакции. Показатель, с которым данный реагент входит в уравнение, называют порядком реакции по веществу (частный порядок реакции), например, показатель а - порядок реакции по веществу А, b - по веществу В. Порядок реакции и молекулярность совпадают только для простых реакций. Определяют порядок реакции те вещества, которые влияют на скорость реакции.
К мономолекулярным относятся реакции разложения и изомеризации.
Реакции, в уравнение скорости которых входит концентрация одного реагирующего вещества в первой степени, называют реакциями первого порядка.
В кинетическое уравнение входят вещества, концентрация которых изменяется в процессе реакции. Концентрации веществ, находящихся в значительном избытке, не изменяются в процессе реакции.
Вода в реакции гидролиза карбоната натрия находится в значительном избытке и в кинетическое уравнение не входит.
В гетерогенных системах столкновение частиц происходит на границе раздела фаз, поэтому масса твердой фазы не влияет на скорость реакции и поэтому не учитывается в выражении для скорости реакции.
К бимолекулярным относятся реакции димеризации и реакции замещения, протекающие через стадию активированного комплекса.
Реакции, скорость которых пропорциональна произведению концентраций двух веществ в первой степени или квадрату концентрации одного вещества, называются реакциями второго порядка.
Тримолекулярные реакции редки, а четырехмолекулярные не известны.
Среди биохимических процессов реакции третьего порядка не встречаются.
Реакции, скорость которых не зависит от концентрации исходных веществ, называются реакциями нулевого порядка (v = k).
Пример реакций нулевого порядка - каталитические реакции, скорость которых зависит только от концентрации катализатора. Частным случаем таких реакций являются ферментативные реакции.
В биохимических процессах участвуют, как правило, несколько реагентов (субстрат, кофермент, кофактор). Иногда не все они известны. Поэтому за ходом процесса судят по одному веществу. При этом количественной характеристикой протекания реакций во времени является период (время) полупревращения реагента - время, за которое количество или концентрация исходного вещества уменьшается в два раза (на 50%) или образуется половина продуктов реакции. Таким способом характеризуют, в частности, распад радионуклидов, так как их период полупревращения не зависит от исходного количества.
Анализируя зависимость периода полупревращения реакции от начальной концентрации, можно определить порядок реакции (способ Оствальда-Нойеса). Постоянством периода полупревращения (при данной температуре) характеризуются многие реакции разложения и вообще реакции первого порядка. С увеличением концентрации реагента период полупревращения уменьшается для реакций второго порядка и увеличивается для реакций нулевого порядка.
2.3. КОНСТАНТА СКОРОСТИ РЕАКЦИИ, ЕЕ ОПРЕДЕЛЕНИЕ. ЗАКОН ДЕЙСТВУЮЩИХ МАСС
Скорость гомогенных реакций зависит от числа встреч реагирующих частиц в единицу времени в единице объема. Вероятность соударения взаимодействующих частиц пропорциональна произведению концентраций реагирующих веществ. Таким образом, скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам соответствующих веществ в уравнении реакции. Указанная закономерность называется законом действующих масс (закон скорости химической реакции), который является
основным законом химической кинетики. Закон действующих масс установлен норвежскими учеными К. Гульдбергом и П. Ваге в 1867 г.
Например, для реакции, протекающей в общем виде, согласно схеме
будет справедливо кинетическое уравнение:
где v - скорость химической реакции; с А и с В - концентрации веществ А и В [моль/л]; v a и v b - показатели порядка по реагентам A и B; k - константа скорости химической реакции - коэффициент, не зависящий от концентрации реагирующих веществ.
Константа скорости химической реакции (k) представляет собой скорость химической реакции в условиях, когда произведение концентраций реагирующих веществ равно 1 моль/л. В этом случае v = k.
Например, если в реакции Н 2 (г) + I 2 (г) = 2НI(г) c(H 2) и c(I 2) равны по 1 моль/л или если c(H 2) равна 2 моль/л, а c(I 2) 0,5 моль/л, то v = k.
Единицы измерения константы равновесия определяются стехиометрией реакции. Константы скорости реакций разных порядков сравнивать между собой некорректно, поскольку они являются разными по смыслу величинами, имеющими разные размерности.
2.4. МЕХАНИЗМ ХИМИЧЕСКИХ РЕАКЦИЙ. КЛАССИФИКАЦИЯ СЛОЖНЫХ РЕАКЦИЙ
Механизм реакций рассматривает все столкновения индивидуальных частиц, которые происходят одновременно или последовательно. Механизм дает детальную стехиометрическую картину каждой ступени реакции, т.е. понимание механизма означает установление молеку-лярности каждой ступени реакции. Изучение механизма химических реакций является очень сложной задачей. Ведь мы же не можем проводить прямые наблюдения за ходом взаимодействия молекул. Полученные результаты иногда зависят от размеров и формы сосуда. В некоторых случаях одни и те же результаты можно объяснить, используя разные механизмы.
Реакция газообразных водорода с йодом Н 2 (г) + I 2 (г) = 2НI(г) считалась классическим примером бимолекулярной реакции второго
порядка, но в 1967 г. Н.Н. Семенов, Г. Эйринг и Дж. Салливэн показали, что она имеет сложный характер и состоит из 3 элементарных реакций: I 2 = 2I; 2I = I 2 ; 2I + H 2 = 2HI. Хотя реакция формально может быть отнесена к тримолекулярным, ее скорость описывается кинетическим уравнением, напоминающим уравнение реакции второго порядка:

В сложных реакциях молекулярность и порядок реакции, как правило, не совпадают. Необычный - дробный или отрицательный - порядок реакции однозначно указывает на ее сложный механизм.
Кинетическое уравнение реакции окисления угарного газа кислородом 2СО(г) + O 2 (г) = СO 2 (г) имеет отрицательный (минус первый) порядок по СО:
при увеличении концентрации угарного газа скорость реакции уменьшается.
По механизму протекания реакции можно разделить на несколько типов.
Последовательными реакциями называют сложные реакции, в каждой из которых продукт (Х 1) первой элементарной стадии вступает в реакцию с продуктом второй стадии, продукт (Х 2) второй стадии вступает в третью и т.д., пока не образуется конечный продукт:

где S - субстрат (исходный реагент); k 1 , k 2 , k 3 ... - константа скорости 1, 2 и т.д. стадий реакции; P - конечный продукт.
Стадии последовательных реакций протекают с различной скоростью. Стадия, константа скорости которой минимальна, называется лимитирующей. Она определяет кинетическую закономерность реакции в целом. Вещества, образующиеся в промежуточных стадиях, называются промежуточными продуктами или интермедиатами, которые являются субстратами последующих стадий. Если интермедиат медленно образуется и быстро распадается, то его концентрация в течение длительного времени не изменяется. Практически все процессы метаболизма являются последовательными реакциями (например, метаболизм глюкозы).
Параллельными реакциями называют реакции, имеющие одни и те же исходные реагенты, которым соответствуют различные продукты. Скорость параллельных реакций равна сумме скоростей отдельных реакций. Это правило применимо и для бимолекулярных параллельных химических реакций.
Последовательно-параллельными реакциями называют реакции, имеющие одни и те же исходные реагенты, которые могут реагировать по двум путям (механизмам) и более, в том числе с разным количеством промежуточных стадий. Данный случай лежит в основе явления катализа, когда интермедиат одного из путей будет способствовать увеличению скорости других путей.
Конкурирующими реакциями называют сложные реакции, в которых одно и тоже вещество А одновременно взаимодействует с одним или несколькими реагентами В 1 , В 2 и т.д., участвует в одновременно протекающих реакциях: А + В 1 → Х 1 ; А + В 2 → Х 2 . Эти реакции конкурируют друг с другом за реагент А.
Сопряженными реакциями называют сложные реакции, в которых одна реакция протекает только в присутствии другой. В сопряженных реакциях промежуточное вещество служит связывающим звеном между первичным и вторичным процессами и обусловливает протекание обоих.
Живая клетка для своего существования нуждается в энергии. Универсальным источником энергии в живых организмах является аде-нозинтрифосфорная кислота (АТФ). Это соединение выполняет функцию аккумулятора энергии, так как при его взаимодействии с водой, т.е. гидролизе, образуются аденозиндифосфорная (АДФ) и фосфорная (Ф) кислоты и выделяется энергия. Поэтому АТФ называется макро-эргическим соединением, а разрывающаяся при его гидролизе связь Р-О-Р - макроэргической. Макроэргической связью называется химическая связь, при разрыве которой в результате реакции гидролиза выделяется значительная энергия:
Как известно, разрыв любой связи (в том числе и макроэргической) всегда требует затраты энергии. В случае же гидролиза АТФ, кроме процесса разрыва связи между фосфатными группами, для которого ΔG >0, происходят процессы гидратации, изомеризации и нейтрализации продуктов, образующихся при гидролизе. В результате всех этих процессов суммарное изменение энергии Гиббса имеет отрицательное
значение. Следовательно, макроэргическим является не разрыв связи, а энергетический результат ее гидролиза.
Для того чтобы в живых системах протекали эндэргонические реакции (ΔG >0), необходимо, чтобы они были сопряжены с экзэрго-ническими реакциями (ΔG <0). Такое сопряжение возможно, если обе реакции имеют какое-либо общее промежуточное соединение, и на всех стадиях сопряженных реакций суммарный процесс характеризуется отрицательным значением изменения энергии Гиббса (∑ΔG сопр.р <0). Например, синтез сахарозы является эндэргонической реакцией и самопроизвольно происходить не может:
Однако сопряжение этой реакции с экзэргонической реакцией гидролиза АТФ, сопровождающееся образованием общего промежуточного соединения глюкозо-1-фосфата, приводит к тому, что суммарный процесс имеет ∑ΔG <0:
Цепными реакциями называют химические и ядерные реакции, в которых появление активной частицы (свободного радикала или атома в химических, нейтрона в ядерных процессах) вызывает большое число (цепь) последовательных превращений неактивных молекул или ядер. Цепные реакции распространены в химии. По цепному механизму протекают многие фотохимические реакции, процессы окисления (горение, взрыв), полимеризации, крекинга. Теория цепных реакций разработана академиком H.H. Семеновым, С.Н. Хиншельвудом (Англия) и др. Основными стадиями цепных реакций являются: зарождение (инициация), продолжение (элонгация) и обрыв цепи (терминация). Различают два типа цепных реакций: реакции с неразветвленными и с разветвленными цепями. Особенность цепных реакций состоит в том, что один первичный акт активации приводит к превращению огромного числа молекул исходных веществ. Биохимические реакции свободно-радикального окисления являются цепными.
Периодическими (автоколебательными) реакциями называют сложные многостадийные автокаталитические реакции с участием нескольких веществ, в которых происходит периодическое колебание концентраций окисленной и восстановленной форм. Колебательные реакции открыты Б.П. Белоусовым, исследованы А.М. Жаботинским и др. Частота и форма колебаний зависят от концентраций исходных веществ, кислот-
ности, температуры. Примером таких реакций может являться взаимодействие броммалоновой кислоты с броматом калия в кислой среде, катализатором служит соль церия (III). Периодические реакции имеют большое значение для биологических объектов, где реакции подобного рода широко распространены.
Реакции твердофазного горения (реакции самораспространяющегося высокотемпературного синтеза, СВС) открыты в 1967 году в Институте химической физики АН СССР А.Г. Мержановым и И.Г. Боровинской. Сущность метода СВС заключается в том, что после локального инициирования реакции взаимодействия реагентов фронт реакции горения самопроизвольно распространяется по всей системе благодаря теплопередаче от горячих продуктов к исходным веществам, инициируя протекание в них реакции взаимодействия. Таким образом, осуществляется процесс горения, который является и причиной, и следствием протекания реакции. Механизм протекания реакций СВС является достаточно сложным и включает в себя процессы реакционной диффузии. Термин «реакционная диффузия» определяет совокупность явлений, происходящих при взаимодействии двух химически различных компонентов, способных образовывать химические соединения в виде твердых фаз. Продукты химического взаимодействия образуют сплошной слой, отличающийся по своему строению от исходных компонентов, но не мешающий протеканию дальнейшего взаимодействия.
2.5. ТЕОРИЯ АКТИВНЫХ СОУДАРЕНИЙ. ЭНЕРГИЯ АКТИВАЦИИ. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ПРИРОДЫ РЕАГИРУЮЩИХ ВЕЩЕСТВ И ТЕМПЕРАТУРЫ
Для того чтобы совершился элементарный акт химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако не каждое столкновение приводит к химическому взаимодействию. Последнее происходит в том случае, когда частицы приближаются на расстояния, при которых возможно перераспределение электронной плотности и возникновение новых химических связей. Взаимодействующие частицы должны обладать энергией, достаточной для преодоления сил отталкивания, возникающих между их электронными оболочками.
Переходное состояние - состояние системы, при котором уравновешены разрушение и создание связи. В переходном состоянии система
находится в течение небольшого (10 -15 с) времени. Энергия, которую необходимо затратить, чтобы привести систему в переходное состояние, называется энергией активации. В многоступенчатых реакциях, которые включают в себя несколько переходных состояний, энергия активации соответствует наибольшему значению энергии. После преодоления переходного состояния молекулы вновь разлетаются с разрушением старых связей и образованием новых или с преобразованием исходных связей. Оба варианта возможны, так как происходят с высвобождением энергии. Существуют вещества, способные уменьшить энергию активации для данной реакции.
Активные молекулы А 2 и B 2 при столкновении объединяются в промежуточный активный комплекс А 2 ...В 2 с ослаблением, а затем и разрывом связей А-А и В-В и упрочнением связей А-В.

«Энергия активации» реакции образования HI (168 кДж/моль) значительно меньше, чем энергия, необходимая для полного разрыва связи в исходных молекулах Н 2 и I 2 (571 кДж/моль). Поэтому путь реакции через образование активного (активированного) комплекса энергетически более выгоден, чем путь через полный разрыв связей в исходных молекулах. Через образование промежуточных активных комплексов происходит подавляющее большинство реакций. Положения теории активного комплекса разработаны Г. Эйрингом и М. Поляни в 30 годах XX в.
Энергия активации представляет собой избыток кинетической энергии частиц относительно средней энергии, необходимой для химического превращения сталкивающихся частиц. Реакции характеризуются различными величинами энергии активации (Е а). В большинстве случаев энергия активации химических реакций между нейтральными молекулами составляет от 80 до 240 кДж/моль. Для биохимических процессов значения Е а зачастую ниже - до 20 кДж/моль. Это объясняется тем, что абсолютное большинство биохимических процессов протекает через стадию фермент-субстратных комплексов. Энергетические барьеры ограничивают протекание реакции. Благодаря этому в принципе возможные реакции (при G <0) практически всегда не протекают
или замедляются. Реакции с энергией активации выше 120 кДж/моль настолько медленны, что их протекание трудно заметить.
Для осуществления реакции молекулы при столкновении должны быть определенным образом ориентированы и обладать достаточной энергией. Вероятность надлежащей ориентации при столкновении характеризуют с помощью энтропии активации ΔS a . Перераспределению электронной плотности в активном комплексе благоприятствует условие, когда при столкновении молекулы А 2 и В 2 ориентированы, как это показано на рис. 2.2, а, тогда как при ориентации, показанной на рис. 2.2, б, вероятность реакции еще гораздо меньше - на рис. 2.2, в.

Рис. 2.2. Благоприятная (а) и неблагоприятные (б, в) ориентации молекул А 2
и В 2 при столкновении
Уравнение, характеризующее зависимость скорости и реакции от температуры, энергии активации и энтропии активации, имеет вид:
где k - константа скорости реакции; A - в первом приближении общее число столкновений между молекулами за единицу времени (секунду) в единице объема; е - основание натуральных логарифмов; R - универсальная газовая постоянная; Т - абсолютная температура; Е а - энергия активации; ΔS a - изменение энтропии активации.
Уравнение (2.8) выведено Аррениусом в 1889 году. Предэкспо-ненциальный множитель A пропорционален общему числу соударений между молекулами в единицу времени. Его размерность совпадает с размерностью константы скорости и, следовательно, зависит от суммарного порядка реакции. Экспонента равна доле активных соударений от их общего числа, т.е. столкнувшиеся молекулы должны иметь доста-
точную энергию взаимодействия. Вероятность же их нужной ориентации в момент соударения пропорциональна e ΔSa/R
При обсуждении закона действующих масс для скорости (2.6) специально было оговорено, что константа скорости есть постоянная величина, не зависящая от концентраций реагентов. При этом предполагалось, что все химические превращения протекают при постоянной температуре. Вместе с тем хорошо известно, что быстрота химического превращения может существенно изменяться при понижении или повышении температуры. С точки зрения закона действующих масс это изменение скорости обусловлено температурной зависимостью константы скорости, так как концентрации реагирующих веществ лишь незначительно меняются вследствие теплового расширения или сжатия жидкости.
Наиболее хорошо известным фактом является возрастание скорости реакций с увеличением температуры. Такой тип температурной зависимости скорости называется нормальным (рис. 2.3, а). Этот тип зависимости характерен для всех простых реакций.

Рис. 2.3. Типы температурной зависимости скорости химических реакций: а - нормальная; б - аномальная; в - ферментативная
Однако в настоящее время хорошо известны химические превращения, скорость которых падает с увеличением температуры. В качестве примера можно привести газофазную реакцию азота (II) оксида с бромом (рис. 2.3, б). Такой тип температурной зависимости скорости называется аномальным.
Особый интерес для медиков представляет зависимость от температуры скорости ферментативных реакций, т.е. реакций с участием ферментов. Практически все реакции, протекающие в организме, относятся к этому классу. Например, при разложении водородперок-сида в присутствии фермента каталазы скорость разложения зависит от температуры. В интервале 273-320 °K температурная зависимость имеет нормальный характер. С увеличением температуры скорость возрастает, с уменьшением - падает. При подъеме температуры выше
320 °K наблюдается резкое аномальное падение скорости разложения пероксида. Сходная картина имеет место и для других ферментативных реакций (рис. 2.3, в).
Из уравнения Аррениуса для k видно, что, поскольку Т входит в показатель степени, скорость химической реакции очень чувствительна к изменению температуры. Зависимость скорости гомогенной реакции от температуры может быть выражена правилом Вант-Гоффа, согласно которому при увеличении температуры на каждые 10° скорость реакции возрастает в 2-4 раза; число, показывающее во сколько раз возрастает скорость данной реакции при повышении температуры на 10°, называется температурным коэффициентом скорости реакции - γ.
где k - константа скорости при температуре t °C. Зная величину γ, можно рассчитать изменение скорости реакции при изменении температуры от T 1 до T 2 по формуле:
При повышении температуры в арифметической прогрессии скорость возрастает в геометрической.
Например, если γ = 2,9, то при возрастании температуры на 100° скорость реакции увеличивается в 2,9 10 раз, т.е. в 40 тыс. раз. Отклонения от этого правила составляют биохимические реакции, скорость которых увеличивается в десятки раз при незначительном повышении температуры. Это правило справедливо лишь в грубом приближении. Реакции, в которых участвуют крупные молекулы (белка), характеризуются большим температурным коэффициентом. Скорость денатурации белка (яичного альбумина) возрастает в 50 раз при повышении температуры на 10 °С. После достижения некоторого максимума (50-60 °С) скорость реакции резко понижается в результате термоденатурации белка.
Для многих химических реакций закон действующих масс для скорости неизвестен. В таких случаях для описания температурной зависимости скорости превращения может применяться выражение:
Предэкспонента А с не зависит от температуры, однако зависит от концентрации. Единицей измерения является моль/л с.
Теоретическая зависимость позволяет заранее рассчитывать скорость при любой температуре, если известны энергия активации и предэкспонента. Таким образом, прогнозируется влияние температуры на быстроту протекания химического превращения.
2.6. ОБРАТИМЫЕ И НЕОБРАТИМЫЕ РЕАКЦИИ. СОСТОЯНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ. УРАВНЕНИЕ ИЗОТЕРМЫ РЕАКЦИИ
Химическая реакция не всегда «доходит до конца», другими словами, исходные вещества не всегда полностью превращаются в продукты реакции. Это происходит потому, что по мере накопления продуктов реакции могут создаться условия для протекания реакции в противоположном направлении. Действительно, если, например, смешать пары йода с водородом при температуре ~200 °С, то произойдет реакция: Н 2 + I 2 = 2HI. Однако известно, что йодоводород уже при нагревании до 180 °С начинает разлагаться на йод и водород: 2HI = Н 2 + I 2 .
Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называют обратимыми. При написании уравнений обратимых реакций вместо знака равенства ставят две противоположно направленные стрелки. Реакцию, протекающую слева направо, называют прямой (константа скорости прямой реакции k 1), справа налево - обратной (константа скорости обратной реакции k 2).
В обратимых реакциях скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие уменьшения концентрации исходных веществ. И наоборот, обратная реакция в начальный момент имеет минимальную скорость, которая увеличивается по мере нарастания концентрации продуктов реакции. Наконец, наступает такой момент, когда скорости прямой и обратной реакции становятся равными. Состояние, в котором скорость обратной реакции становится равной скорости прямой реакции, называют химическим равновесием.
Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. В момент достижения состояния химического равновесия скорости прямой и обратной реакций равны (кинетическое условие).
где K - константа равновесия, представляющая собой отношение констант скорости прямой и обратной реакций.
В правой части уравнения стоят те концентрации взаимодействующих веществ, которые устанавливаются при равновесии - равновесные концентрации. Это уравнение представляет собой математическое выражение закона действующих масс при химическом равновесии. Особо следует отметить, что в отличие от закона действующих масс для скорости реакции в данном уравнении показатели степени a, b, d, f и т.д. всегда равны стехиометрическим коэффициентам в равновесной реакции.
Численное значение константы равновесия данной реакции определяет ее выход. Выходом реакции называют отношение количества получаемого в действительности продукта к тому количеству, которое получилось бы при протекании реакции до конца (выражается обычно в процентах). Так, при K >>1 выход реакции велик и, наоборот, при K <<1 выход реакции очень мал.
Константа равновесия связана со стандартной энергией Гиббса реакции следующим соотношением:
Используя уравнение (2.12), можно найти значение энергии Гиббса реакции через равновесные концентрации:

Это уравнение называют уравнением изотермы химической реакции. Оно позволяет рассчитать изменение энергии Гиббса при протекании процесса и определить направление протекания реакции:
при ΔG <0 - реакция идет в прямом направлении, слева направо;
При ΔG = 0 - реакция достигла равновесия (термодинамическое условие);
при ΔG >0 - реакция идет в обратном направлении.
Важно понять, что константа равновесия не зависит от концентраций веществ. Справедливо обратное утверждение: в состоянии равновесия сами концентрации принимают такие значения, что отношение их произведений в степенях стехиометрических коэффициентов
оказывается постоянной величиной при данной температуре. Данное утверждение соответствует закону действующих масс и даже может использоваться в качестве одной из его формулировок.
Как было сказано выше, обратимые реакции не протекают до конца. Однако если один из продуктов обратимой реакции покидает сферу реакции, то по существу обратимый процесс протекает практически до конца. Если в обратимой реакции участвуют электролиты и один из продуктов этой реакции представляет собой слабый электролит, осадок или газ, то в этом случае реакция также протекает практически до конца. Необратимыми реакциями называют такие реакции, продукты которых не взаимодействуют друг с другом с образованием исходных веществ. Необратимые реакции, как правило, «доходят до конца», т.е. до полного израсходования хотя бы одного из исходных веществ.
2.7. ПРИНЦИП ЛЕ ШАТЕЛЬЕ
Состояние химического равновесия при неизменных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности при изменении температуры, давления или концентрации реагентов равновесие может «сместиться» в ту или иную сторону протекания процесса.
Изменения, происходящие в системе в результате внешних воздействий, определяются принципом подвижного равновесия - принципом Ле Шателье.
Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Применительно к трем основным типам внешнего воздействия - изменению концентрации, давления и температуры - принцип Ле Шателье трактуется следующим образом.
При увеличении концентрации одного из реагирующих веществ равновесие смещается в сторону расхода этого вещества, при уменьшении концентрации равновесие смещается в сторону образования этого вещества.
Влияние давления очень напоминает эффект изменения концентраций реагирующих веществ, но сказывается оно только на газовых системах. Сформулируем общее положение о влиянии давления на химическое равновесие.
При увеличении давления равновесие смещается в сторону уменьшения количеств газообразных веществ, т.е. в сторону понижения давления; при уменьшении давления равновесие смещается в сторону возрастания
количеств газообразных веществ, т.е. в сторону увеличения давления. Если реакция протекает без изменения числа молекул газообразных веществ, то давление не влияет на положение равновесия в этой системе.
При изменении температуры изменяются как прямая, так и обратная реакции, но в разной степени. Следовательно, для выяснения влияния температуры на химическое равновесие необходимо знать знак теплового эффекта реакции.
При повышении температуры равновесие смещается в сторону эндотермической реакции, при понижении температуры - в сторону экзотермической реакции.
Применительно к биосистемам принцип Ле Шателье гласит, что в биосистеме на каждое действие формируется такое же по силе и характеру противодействие, которое уравновешивает биологические регуляторные процессы и реакции и формирует сопряженный уровень их неравновесности.
При патологических процессах существующая замкнутость регу-ляторного контура нарушается. В зависимости от уровня неравновесности изменяется качество межсистемных и межорганных отношений, они приобретают все более нелинейный характер. Структуру и специфику этих взаимоотношений подтверждает анализ зависимости между показателями системы перекисного окисления липидов и уровнем антиоксидантов, между гармоническими показателями в условиях адаптации и патологии. Данные системы участвуют в поддержании антиокислительного гомеостаза.
2.8. ВОПРОСЫ И ЗАДАЧИ ДЛЯ САМОПРОВЕРКИ ПОДГОТОВЛЕННОСТИ К ЗАНЯТИЯМ И ЭКЗАМЕНАМ
1.Какие реакции называются гомогенными, а какие гетерогенными? Приведите по одному примеру каждого типа реакций.
2.Какие реакции называют простыми, а какие сложными? Приведите по два примера простых и сложных реакций.
3.В каком случае молекулярность и порядок кинетического уравнения могут численно совпадать?
4.Скорость некоторой реакции с течением времени не изменяется. Изменится ли с течением времени период полупревращения этой реакции, и если изменится, то как? Дайте объяснение.
5.В каком случае истинная (мгновенная) скорость и средняя скорость реакции (в достаточно большом интервале времени) могут совпадать?
6.Вычислите константу скорости реакции A + B → AB, если при концентрациях веществ A и B, равных соответственно 0,5 и 0,1 моль/л, ее скорость равна 0,005 моль/л мин.
7.Период полупревращения некоторой реакции первого порядка равен 30 мин. Какая часть от первоначального количества вещества останется через час?
8.Дать понятие общего порядка реакции и порядка реакции по веществу.
9.Методы определения скорости реакции.
10.Основной закон химической кинетики.
11.Дать понятие механизма химических реакций.
12.Простые и сложные реакции.
13.Сопряженные реакции. От каких факторов зависит константа скорости химических реакций?
14.Скорость реакции действительно пропорциональна произведению концентраций реагирующих веществ в степени их стехиометри-ческих коэффициентов?
15.Какие требуются экспериментальные данные для определения порядка реакций?
16.Напишите кинетическое уравнение реакции H 2 O 2 + 2HI → I 2 + + 2H 2 O, если смешаны равные объемы 0,02 моль/л раствора H 2 O 2 и 0,05 моль/л раствора HI. Константа скорости 0,05 л/моль с.
17.Напишите кинетическое уравнение реакции H 2 O 2 + 2HI → I 2 + + 2H 2 O, учитывая, что она характеризуется первым порядком реакции по концентрациям обоих исходных веществ.
18.Докажите, что скорость химической реакции максимальна при стехиометрическом соотношении компонентов.
19.Перечислите возможные объяснения влияния температуры на скорость реакции.
2.9. ТЕСТОВЫЕ ЗАДАНИЯ
1. Согласно правилу Вант-Гоффа при повышении температуры на 10° скорость многих реакций:
а)уменьшается в 2-4 раза;
б)уменьшается в 5-10 раз;
в)увеличивается в 2-4 раза;
г)увеличивается в 5-10 раз.
2. Количество элементарных актов взаимодействия в единицу времени определяет:
а)порядок реакции;
б)скорость реакции;
в)молекулярность реакции;
г)период полупревращения.
3. Какие факторы влияют на увеличение скорости реакции?
а)природа реагирующих веществ;
б)температура, концентрация, катализатор;
в)только катализатор;
г)только концентрация;
д)только температура.
4. Во сколько раз увеличится скорость реакции 2А(г) + В(г) → А 2 В(г) при увеличении концентрации вещества А в 2 раза?
а)скорость не изменится;
б)увеличится в 18 раз;
в)увеличится в 8 раз;
г)увеличится в 4 раза;
д)увеличится в 2 раза.
5. Элементарная реакция А(тв) + 2В(г) → АВ 2 (г). Укажите правильное кинетическое уравнение этой реакции:
а)k[A][B] 2 ;
б)k[A][B];
в)к[В];
г)к[В] 2 ;
д)к[А].
6. Как нужно изменить давление в системе, чтобы увеличить скорость реакции А(тв) + 2В(г) → АВ 2 (г) в 9 раз?
а)увеличить давление в 9 раз;
б)уменьшить давление в 9 раз;
в)увеличить давление в 3 раза;
г)уменьшить давление в 3 раза.
7. Чему равен температурный коэффициент реакции γ 10 , если при охлаждении реакционной смеси на 30° скорость реакции уменьшилась в 8 раз?
а)16;
б)8;
в)6;
г)4;
д)2.
8. Какая реакция идет быстрее?
а)Е акт = 40 кДж/моль;
б) Е акт = 80 кДж/моль;
в) Е акт = 160 кДж/моль;
г) Е акт = 200 кДж/моль.
Множитель k в кинетических уравнениях (1.3)- (1.8), показывающий, c какой скоростью идет процесс при концентрациях реагирующих веществ, равных единице, называется константой скорости химического процесса.
Наряду со скоростью константа скорости химического процесса является основным параметром в химической кинетике.
Константы скорости реакций различного порядка имеют неодинаковую размерность. Из уравнения (1.5) следует, что размерность константы скорости для реакции первого порядка t -1 ; из уравнения (1.7) – размерность константы скорости второго порядка c -1 t -1 ; константа скорости третьего порядка, как следует из уравнения (1.8), имеет размерность c -2 t -1 , где c -концентрация, t - время.
Концентрацию обычно измеряют в моль/л , а время в секундах (с ). Тогда размерность константы скорости первого порядка с -1 , второго – л.моль -1 с -1 , третьего – л 2 .моль -2 .с -1 .
Константа скорости реакции зависит от того, по какому соединению она измерена. Например, в реакции димеризации диоксида азота
скорость исчезновения NO 2 вдвое больше скорости появления N 2 O 4 .

Уравнение Аррениуса
Константа скорости химической реакции, как правило, резко возрастает с увеличением температуры. Обычно увеличение температуры реакционной смеси на 10°С приводит к возрастанию скорости реакции в 2-4 раза. Зависимость константы скорости реакции от температуры в большинстве случаев может быть описана уравнением Аррениуса
 ,
(1.9)
,
(1.9)
где E a - энергия активации;
R - универсальная газовая постоянная, равная 8.3 Дж/(моль.К),
А - предэкспоненциальный множитель - частотный фактор, имеющий размерность константы скорости.
Чем больше величина E a , тем быстрее растет скорость реакции с температурой. Если реакции простые, величина E a показывает, какой минимальной избыточной энергией в расчете на 1 моль должны обладать реагирующие частицы, чтобы они могли вступить в реакцию. Частицы, энергия которых больше или равна E a , называются активными.
Для сложных реакций, состоящих из нескольких стадий, параметр E a в уравнении (1.9) не всегда имеет простой физический смысл и часто является некоторой функцией энергии активации отдельных стадий. Тем не менее, и в этом случае параметр E a принято считать энергией активации, хотя правильнее называть его эффективной или эмпирической энергией активации.
Параметры Е а и А могут быть определены из зависимости константы скорости реакции от температуры с помощью уравнения (1.9), записанного в виде:
![]() (1.10)
(1.10)
Из графика зависимости ln k от 1/Т (рис. 1.2) легко находят ln А и E а / R , а из них А и E а. В принципе для определения E а и А достаточно знать константы скорости k 1 и k 2 при двух значениях температуры Т 1 и Т 2

Рисунок 1.2- Аррениусовская зависимость скорости реакции от температуры

Тогда, согласно уравнению (1.10)
Такое определение Е a , как правило, не обеспечивает достаточной точности, и рекомендуется определение энергии активации проводить не менее чем по четырем значениям константы скорости при четырех различных температурах в интервале не менее 30-40 °С.
Нулевой порядок реакции
При проведении гомогенного нитрования бензола, толуола, этилбензола большим избытком азотной кислоты (5 молей НNО 3 на 0.1 моля нитруемого соединения) было обнаружено, что скорость нитрования остается неизменной, пока все нитруемое соединение не прореагирует.
Следовательно, реакция имеет нулевой порядок:
Величина константы скорости нитрования бензола, толуола и этилбензола в этих условиях одинакова и не зависит от концентрации нитруемого соединения. Это объясняется тем, что скорость образования нитроний-катиона в процессе автопротолиза азотной кислоты ниже скорости нитрования ароматического соединения:

а поскольку азотная кислота присутствует в большом избытке, ее концентрация прак-тически не изменяется в ходе реакции.
1. Основные понятия и постулаты химической кинетики
Химическая кинетика - раздел физической химии, изучающий скорости химических реакций. Основные задачи химической кинетики: 1) расчет скоростей реакций и определение кинетических кривых, т.е. зависимости концентраций реагирующих веществ от времени (прямая задача ); 2) определение механизмов реакций по кинетическим кривым (обратная задача ).
Скорость химической реакции описывает изменение концентраций реагирующих веществ в единицу времени. Для реакции
a A + b B + ...d D + e E + ...
скорость реакции определяется следующим образом:
где квадратные скобки обозначают концентрацию вещества (обычно измеряется в моль/л), t - время; a , b , d , e - стехиометрические коэффициенты в уравнении реакции.
Скорость реакции зависит от природы реагирующих веществ, их концентрации, температуры и наличия катализатора. Зависимость скорости реакции от концентрации описывается основным постулатом химической кинетики - законом действующих масс :
Скорость химической реакции в каждый момент времени пропорциональна текущим концентрациям реагирующих веществ, возведенным в некоторые степени:
![]() ,
,
где k - константа скорости (не зависящая от концентрации); x , y - некоторые числа, которые называют порядком реакции по веществам A и B, соответственно. Эти числа в общем случае никак не связаны с коэффициентами a и b в уравнении реакции. Сумма показателей степеней x + y называется общим порядком реакции . Порядок реакции может быть положительным или отрицательным, целым или дробным.
Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями . Под элементарной реакцией обычно понимают единичный акт образования или разрыва химической связи, протекающий через образование переходного комплекса. Число частиц, участвующих в элементарной реакции, называют молекулярностью реакции. Элементарные реакции бывают только трех типов: мономолекулярные (A B + ...), бимолекулярные (A + B D + ...) и тримолекулярные (2A + B D + ...). Для элементарных реакций общий порядок равен молекулярности, а порядки по веществам равны коэффициентам в уравнении реакции.
ПРИМЕРЫ
Пример 1-1. Скорость образования NO в реакции 2NOBr (г) 2NO (г) + Br 2(г) равна 1.6 . 10 -4 моль/(л. с). Чему равна скорость реакции и скорость расходования NOBr?
Решение . По определению, скорость реакции равна:
Моль/(л. с).
Из этого же определения следует, что скорость расходования NOBr равна скорости образования NO с обратным знаком:
![]() моль/(л. с).
моль/(л. с).
Пример 1-2. В реакции 2-го порядка A + B D начальные концентрации веществ A и B равны, соответственно, 2.0 моль/л и 3.0 моль/л. Скорость реакции равна 1.2 . 10 -3 моль/(л. с) при [A] = 1.5 моль/л. Рассчитайте константу скорости и скорость реакции при [B] = 1.5 моль/л.
Решение . По закону действующих масс, в любой момент времени скорость реакции равна:
![]() .
.
К моменту времени, когда [A] = 1.5 моль/л, прореагировало по 0.5 моль/л веществ A и B, поэтому [B] = 3 – 0.5 = 2.5 моль/л. Константа скорости равна:
Л/(моль. с).
К моменту времени, когда [B] = 1.5 моль/л, прореагировало по 1.5 моль/л веществ A и B, поэтому [A] = 2 – 1.5 = 0.5 моль/л. Скорость реакции равна:
Моль/(л. с).
ЗАДАЧИ
1-1. Как выражается скорость реакции синтеза аммиака 1/2 N 2 + 3/2 H 2 = NH 3 через концентрации азота и водорода? (ответ)
1-2. Как изменится скорость реакции синтеза аммиака 1/2 N 2 + 3/2 H 2 = NH 3 , если уравнение реакции записать в виде N 2 + 3H 2 = 2NH 3 ? (ответ)
1-3. Чему равен порядок элементарных реакций: а) Сl + H 2 = HCl + H; б) 2NO + Cl 2 = 2NOCl? (ответ)
1-4. Какие из перечисленных величин могут принимать а) отрицательные; б) дробные значения: скорость реакции, порядок реакции, молекулярность реакции, константа скорости, стехиометрический коэффициент? (ответ)
1-5. Зависит ли скорость реакции от концентрации продуктов реакции? (ответ)
1-6. Во сколько раз увеличится скорость газофазной элементарной реакции A = 2D при увеличении давления в 3 раза?(ответ)
1-7. Определите порядок реакции, если константа скорости имеет размерность л 2 /(моль 2 . с). (ответ)
1-8. Константа скорости газовой реакции 2-го порядка при 25 о С равна 10 3 л/(моль. с). Чему равна эта константа, если кинетическое уравнение выражено через давление в атмосферах?(ответ)
1-9. Для газофазной реакции n -го порядка nA B выразите скорость образования B через суммарное давление.(ответ)
1-10. Константы скорости прямой и обратной реакции равны 2.2 и 3.8 л/(моль. с). По какому из перечисленных ниже механизмов могут протекать эти реакции: а) A + B = D; б) A + B = 2D; в) A = B + D; г) 2A = B.(ответ)
1-11. Реакция разложения 2HI H 2 + I 2 имеет 2-й порядок с константой скорости k = 5.95 . 10 -6 л/(моль. с). Вычислите скорость реакции при давлении 1 атм и температуре 600 К. (ответ)
1-12. Скорость реакции 2-го порядка A + B D равна 2.7 . 10 -7 моль/(л. с) при концентрациях веществ A и B, соответственно, 3.0 . 10 -3 моль/л и 2.0 моль/л. Рассчитайте константу скорости.(ответ)
1-13. В реакции 2-го порядка A + B 2D начальные концентрации веществ A и B равны по 1.5 моль/л. Скорость реакции равна 2.0 . 10 -4 моль/(л. с) при [A] = 1.0 моль/л. Рассчитайте константу скорости и скорость реакции при [B] = 0.2 моль/л. (ответ)
1-14. В реакции 2-го порядка A + B 2D начальные концентрации веществ A и B равны, соответственно, 0.5 и 2.5 моль/л. Во сколько раз скорость реакции при [A] = 0.1 моль/л меньше начальной скорости? (ответ)
1-15. Скорость газофазной реакции описывается уравнением w = k . [A] 2 . [B]. При каком соотношении между концентрациями А и В начальная скорость реакции будет максимальна при фиксированном суммарном давлении? (ответ)
2. Кинетика простых реакций
В данном разделе мы составим на основе закона действующих масс и решим кинетические уравнения для необратимых реакций целого порядка.
Реакции 0-го порядка. Скорость этих реакций не зависит от концентрации:
![]() ,
,
где [A] - концентрация исходного вещества. Нулевой порядок встречается в гетерогенных и фотохимических реакциях.
Реакции 1-го порядка. В реакциях типа A B скорость прямо пропорциональна концентрации:
![]() .
.
При решении кинетических уравнений часто используют следующие обозначения: начальная концентрация [A] 0 = a , текущая концентрация [A] = a - x (t ), где x (t ) - концентрация прореагировавшего вещества A. В этих обозначениях кинетическое уравнение для реакции 1-го порядка и его решение имеют вид:
Решение кинетического уравнения записывают и в другом виде, удобном для анализа порядка реакции:
![]() .
.
Время, за которое распадается половина вещества A, называют периодом полураспада t 1/2 . Он определяется уравнением x (t 1/2) = a /2 и равен
Реакции 2-го порядка. В реакциях типа A + B D + ... скорость прямо пропорциональна произведению концентраций:
![]() .
.
Начальные концентрации веществ: [A] 0 = a , [B] 0 = b ; текущие концентрации: [A] = a - x (t ), [B] = b - x (t ).
При решении этого уравнения различают два случая.
1) одинаковые начальные концентрации веществ A и B: a = b . Кинетическое уравнение имеет вид:
![]() .
.
Решение этого уравнения записывают в различных формах:
Период полураспада веществ A и B одинаков и равен:
2) Начальные концентрации веществ A и B различны: a
b
. Кинетическое
уравнение имеет вид:![]() .
.
Решение этого уравнения можно записать следующим образом:
Периоды полураспада веществ A и B различны: ![]() .
.
Реакции n-го порядка n A D + ... Кинетическое уравнение имеет вид:
![]() .
.
Решение кинетического уравнения:
 . (2.1)
. (2.1)
Период полураспада вещества A обратно пропорционален (n -1)-й степени начальной концентрации:
![]() . (2.2)
. (2.2)
Пример 2-1.
Период полураспада
радиоактивного изотопа 14 C - 5730 лет. При
археологических раскопках было найдено дерево,
содержание 14 C в котором составляет 72% от
нормального. Каков возраст дерева?
Решение.
Радиоактивный распад - реакция 1-го
порядка. Константа скорости равна:
Время жизни дерева можно найти из решения кинетического уравнения с учетом того, что [A] = 0.72 . [A] 0:
Пример 2-2.
Установлено, что реакция 2-го
порядка (один реагент) завершается на 75% за 92 мин
при исходной концентрации реагента 0.24 М. Какое
время потребуется, чтобы при тех же условиях
концентрация реагента достигла 0.16 М?
Решение.
Запишем два раза решение
кинетического уравнения для реакции 2-го порядка
с одним реагентом:
![]() ,
,
где, по условию, a = 0.24 M, t 1 = 92 мин, x 1 = 0.75 . 0.24 = 0.18 M, x 2 = 0.24 - 0.16 = 0.08 M. Поделим одно уравнение на другое:
Пример 2-3.
Для элементарной реакции n
A B обозначим
период полураспада A через t 1/2 , а время
распада A на 75% - через t 3/4 . Докажите, что
отношение t 3/4 / t 1/2 не зависит от
начальной концентрации, а определяется только
порядком реакции n
.Решение.
Запишем два раза решение
кинетического уравнения для реакции n
-го
порядка с одним реагентом:
и поделим одно выражение на другое. Постоянные величины k и a из обоих выражений сократятся, и мы получим:
![]() .
.
Этот результат можно обобщить, доказав, что отношение времен, за которые степень превращения составит a и b , зависит только от порядка реакции:
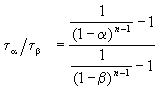 .
.
ЗАДАЧИ
2-1. Пользуясь решением кинетического уравнения, докажите, что для реакций 1-го порядка время t x , за которое степень превращения исходного вещества достигает x , не зависит от начальной концентрации. (ответ)2-2. Реакция первого порядка протекает на 30% за 7 мин. Через какое время реакция завершится на 99%? (ответ)
2-3. Период полураспада радиоактивного изотопа 137 Cs, который попал в атмосферу в результате Чернобыльской аварии, - 29.7 лет. Через какое время количество этого изотопа составит менее 1% от исходного? (ответ)
2-4. Период полураспада радиоактивного изотопа 90 Sr, который попадает в атмосферу при ядерных испытаниях, - 28.1 лет. Предположим, что организм новорожденного ребенка поглотил 1.00 мг этого изотопа. Сколько стронция останется в организме через а) 18 лет, б) 70 лет, если считать, что он не выводится из организма?(ответ)
2-5. Константа скорости для реакции первого порядка SO 2 Cl 2 = SO 2 + Cl 2 равна 2.2 . 10 -5 с -1 при 320 о С. Какой процент SO 2 Cl 2 разложится при выдерживании его в течение 2 ч при этой температуре?(ответ)
2-6. Константа скорости реакции 1-го порядка
2N 2 O 5(г) 4NO 2(г) + O 2(г)
при 25 о С равна 3.38 . 10 -5 с -1 . Чему равен период полураспада N 2 O 5 ? Чему будет равно давление в системе через а) 10 с, б) 10 мин, если начальное давление было равно 500 мм рт. ст. (ответ)
2-7. Реакцию первого порядка проводят с различными количествами исходного вещества. Пересекутся ли в одной точке на оси абсцисс касательные к начальным участкам кинетических кривых? Ответ поясните.(ответ)
2-8. Реакция первого порядка A 2B протекает в газовой фазе. Начальное давление равно p 0 (B отсутствует). Найдите зависимость общего давления от времени. Через какое время давление увеличится в 1.5 раза по сравнению с первоначальным? Какова степень протекания реакции к этому времени? (ответ)
2-9. Реакция второго порядка 2A B протекает в газовой фазе. Начальное давление равно p 0 (B отсутствует). Найдите зависимость общего давления от времени. Через какое время давление уменьшится в 1.5 раза по сравнению с первоначальным? Какова степень протекания реакции к этому времени? (ответ)
2-10. Вещество A смешали с веществами B и C в равных концентрациях 1 моль/л. Через 1000 с осталось 50% вещества А. Сколько вещества А останется через 2000 с, если реакция имеет: а) нулевой, б) первый, в) второй, в) третий общий порядок?(ответ)
2-11. Какая из реакций - первого, второго или третьего порядка - закончится быстрее, если начальные концентрации веществ равны 1 моль/л и все константы скорости, выраженные через моль/л и с, равны 1? (ответ)
2-12. Реакция
CH 3 CH 2 NO 2 + OH - H 2 O + CH 3 CHNO 2 -
имеет второй порядок и константу скорости k = 39.1 л/(моль. мин) при 0 о С. Был приготовлен раствор, содержащий 0.004 М нитроэтана и 0.005 М NaOH. Через какое время прореагирует 90% нитроэтана?
2-13. Константа скорости рекомбинации ионов H + и ФГ - (фенилглиоксинат) в молекулу НФГ при 298 К равна k = 10 11.59 л/(моль. с). Рассчитайте время, в течение которого реакция прошла на 99.999%, если исходные концентрации обоих ионов равны 0.001 моль/л. (ответ)
2-14. Скорость окисления бутанола-1 хлорноватистой кислотой не зависит от концентрации спирта и пропорциональна 2 . За какое время реакция окисления при 298 К пройдет на 90%, если исходный раствор содержал 0.1 моль/л HClO и 1 моль/л спирта? Константа скорости реакции равна k = 24 л/(моль. мин). (ответ)
2-15. При определенной температуре 0.01 М раствор этилацетата омыляется 0.002 М раствором NaOH на 10% за 23 мин. Через сколько минут он будет омылен до такой же степени 0.005 М раствором KOH? Считайте, что данная реакция имеет второй порядок, а щелочи диссоциированы полностью.(ответ)
2-16. Реакция второго порядка A + B P проводится в растворе с начальными концентрациями [A] 0 = 0.050 моль/л и [B] 0 = 0.080 моль/л. Через 1 ч концентрация вещества А уменьшилась до 0.020 моль/л. Рассчитайте константу скорости и периоды полураспада обоих веществ.
- Решить систему сравнений
- Мавритания. Общие впечатления. Мавританцы Наука и культура Мавритании
- Графики линейных функций
- Сфера, вписанная в цилиндр, конус и усеченный конус
- Согласные звуки в русском языке П парный
- Воздействие частот в герцах (Гц) на организм
- Измерение времени реакции подростков и взрослых

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter